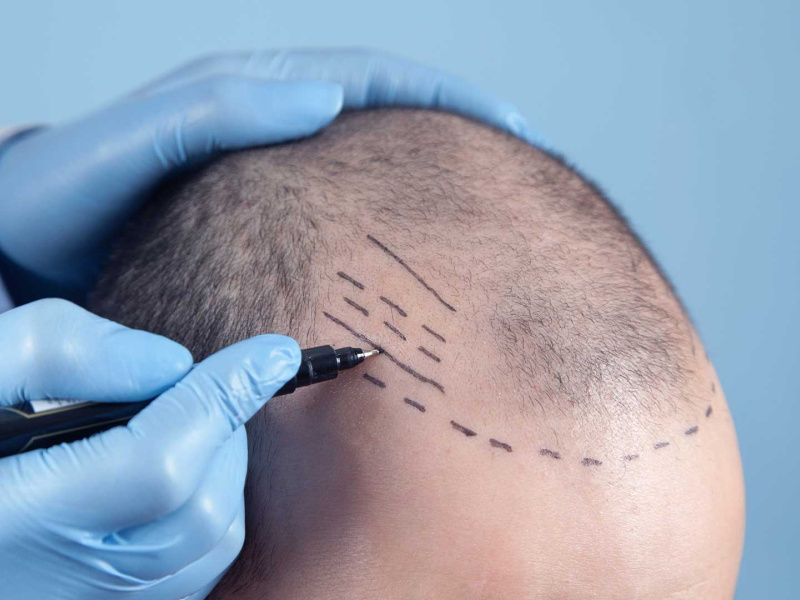
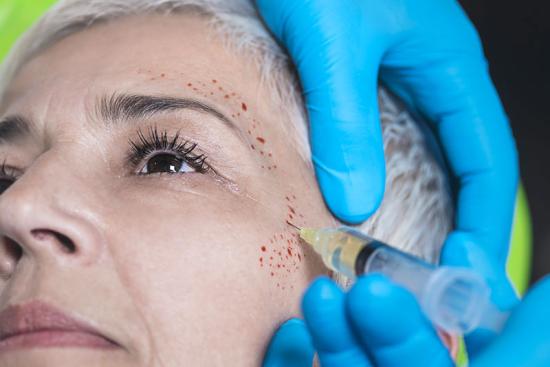
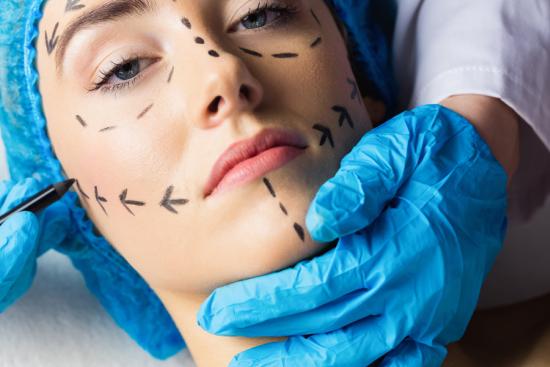
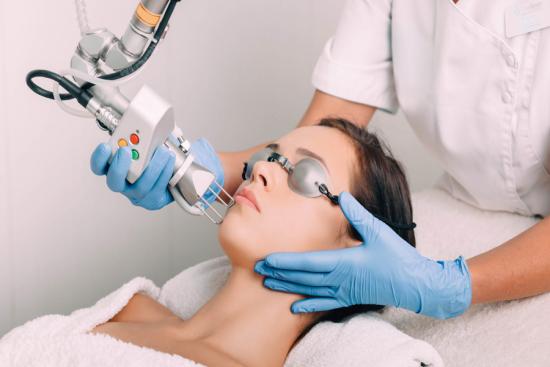
تجديد خلايا الجلد
باستخدام إعادة البرمجة الخلوية، تمكن العلماء من عكس شيخوخة خلايا الجلد بحوالي 30 عامًا، وهي نتيجة غير عادية يمكن أن تؤدي إلى علاجات رائدة لمكافحة الشيخوخة والطب التجديدي في المستقبل، بالإضافة إلى اكتشافات جديدة في مجال علم الوراثة. تم إثبات عمر الخلايا المجددة، التي تم التحقق منها بواسطة قياسات جزيئية محددة، من خلال التحليل السلوكي في جروح الجلد. كان رد فعل هاته الخلايا مشابهًا بالفعل لتفاعل الخلايا التي تقل "على ظهورها" بثلاثة عقود. تعتبر هذه النتائج المعملية أولية تمامًا، لكن التأثير السريري المحتمل لمثل هذا الإجراء قد يكون ثوريًا.
تقنية تجديد الخلايا "الجديدة"
لتجديد خلايا الجلد (الأرومات الليفية)، استخدم الباحثون تقنية إعادة برمجة الخلايا التي طورها ياماناكا ولكن تم "إعادة النظر فيها" وتصحيحها. تتكون هذه التقنية من استخدام نفس الكوكتيل من البروتينات المجددة ، والمعروفة باسم "عوامل Yamanaka" (Oct4 ، Sox2 ، Klf4 و cMyc)، ولكن إعطائها للخلايا لمدة 13 يومًا فقط بدلاً من 50 المتعارف عليها. بهذه الطريقة، تمت إعادة برمجة الخلايا جزئيًا فقط. وبالتالي، تفقد الخلايا جميع العلامات التي تسبب لها الشيخوخة، وتفقد هويتها بشكل مؤقت فقط.
بعد ذلك، تتم زراعة الخلايا المعاد برمجتها جزئيًا في ظل ظروف طبيعية، وبالتالي تستعيد هويتها كخلايا جلدية (مع آلية لم تُكتشف بعد) وقدرتها على إنتاج الكولاجين الخاص بها كما تفعل الخلايا الأصغر سنًا.
الخلايا الليفية والتئام الجروح
وظيفة الخلايا الليفية (خلايا الجلد) هي إنتاج الكولاجين، وهو جزيء موجود في العظام وأوتار الجلد والأربطة، مما يساعد على بناء الأنسجة والتئام الجروح. بفضل تقنية تجديد الخلايا الجديدة التي طورها الباحثون، لا يتم تجديد خلايا الجلد فحسب، بل تعمل أيضًا مثل الخلايا الأصغر سنًا. في الواقع، أنتجت الأرومات الليفية المجددة بروتين كولاجين أكثر من الخلايا الضابطة التي لم تخضع لعملية إعادة البرمجة.
ليس ذلك فحسب، فقد وجد الباحثون، الذين قاموا بفحص الجرح، أن الخلايا الليفية المجددة تهاجر إلى الجرح أسرع من الخلايا غير المعالجة، أي الخلايا القديمة. وقال الباحثون إن هذه إشارة واعدة للطب التجديدي على الأقل فيما يتعلق بعلاج الجروح الجلدية دون ترك ندوب.
الآفاق العلاجية الجديدة
لاحظ الباحثون أن طريقة تجديد الخلايا لديها أيضًا تأثيرات متجددة على الجينات الأخرى المرتبطة بالأمراض والأعراض المرتبطة بالعمر، بما في ذلك جين APBA2 المرتبط بمرض الزهايمر، وجين MAF الذي يساهم في تطور إعتام عدسة العين. . يمكن أن يمهد هذا الطريق لعلاجات جديدة، مع أنّ الآلية الكامنة وراء إعادة البرمجة المؤقتة الناجحة لم يتم فهمها بالكامل بعد. في هذا الصدد، يفترض الباحثون أن مناطق الجينوم الرئيسية المشاركة في تكوين الهوية الخلوية يمكن أن تفلت من عملية إعادة البرمجة.
تمثل النتائج خطوة كبيرة في فهم إعادة البرمجة الخلوية. أظهر الباحثون أن الخلايا يمكن أن تتجدد دون أن تفقد وظيفتها وأن التجديد يحاول استعادة بعض وظائف الخلايا القديمة.